ARTIGO ORIGINAL
A
ADEQUABILIDADE DOS SEGUIMENTOS DE MULHERES COM LAUDOS ALTERADOS EM UM ESTADO DA
AMAZÔNIA LEGAL
THE ADEQUACY OF FOLLOW-UP FOR WOMEN WITH AMENDED REPORTS IN A
LEGAL AMAZON STATE
LA ADECUACIÓN DEL SEGUIMIENTO A MUJERES CON REGISTROS MODIFICADOS
EN UN ESTADO LEGAL DE LA AMAZONÍA
1
Eliane Cristina dos Santos Souza
2
Antonio Matheus Santos Medrado
3
Poliana Guerino Marson
4 Mayenne
Myrcea Quintino Pereira Valente
5 Ana
Caroline Costa da Silva
6
Danielle Rosa Evangelista
1
Biomédica. Especialista em Citologia Oncótica. Mestra em Ciências da Saúde
-Palmas, Tocantins. Orcid: https://orcid.org/0000-0003-1884-7755
2
Enfermeiro pela Universidade Federal do Tocantins – UFT. Mestrando no Programa
de Pós-Graduação em Ensino em Ciências e Saúde – PPGESC – UFT. Palmas,
Tocantins. Orcid: https://orcid.org/0000-0002-3175-1961
3 Docente
da Universidade Federal do Tocantins. Doutorado em Biotecnologia. Graduada em
Farmácia Bioquímica e mestre em Bioquímica, Palmas, Tocantins. Orcid: https://orcid.org/0000-0002-3560-0749
4 Enfermeira.
Especialista em Saúde Pública. Mestra em Enfermagem. Doutorado em Enfermagem.
Professora Adjunto III da Universidade de Fortaleza, Ceará. Orcid: https://orcid.org/0000-0002-2082-4969
5
Enfermeira pela Universidade Federal do Tocantins – UFT, Palmas, Tocantins.
Orcid: https://orcid.org/0000-0003-3675-6275
6 Enfermeira.
Doutora em Enfermagem. Docente do Curso de Graduação em Enfermagem da
Universidade Federal do Tocantins, Palmas, Tocantins. Orcid: https://orcid.org/0000-0002-4472-2879
Autor
correspondente
Danielle
Rosa Evangelista
Endereço:
109 Norte Av. NS-15, ALCNO-14. Plano Diretor Norte. CEP: 77001-090. Palmas/TO -
Brasil, bloco lab 4, sala 03. E-mail: daniellerosa@mail.uft.edu.br
Submissão: 12-09-2022
Aprovado: 25-04-2023
RESUMO
Objetivo:
O presente estudo teve como objetivo verificar a adequabilidade do segmento de
mulheres com laudos alterados no estado do Tocantins. Métodos: Estudo do tipo
transversal, avaliativo e documental. O presente estudo foi desenvolvido no
Estado do Tocantins, o qual possui o SUS organizado pelo princípio da
regionalização e possui 139 municípios. As regiões são: Capim Dourado, Bico do
Papagaio, Amor Perfeito, Ilha do Bananal, Sudeste, Cerrado Tocantins Araguaia,
Médio Norte Araguaia e Cantão. A população adotada foi de 29.531 mulheres,
estimada a partir do levantamento do número de laudos citopatológicos emitidos
durante o ano de 2019. O cálculo amostral considerou a utilização da fórmula
para populações finitas, após aplicação da fórmula, o n ficou em 379
requisições e laudos de mulheres. Buscando ampliar ainda mais a fidedignidade
dos dados, optou-se por triplicar o tamanho amostral, logo o quantitativo ficou
1.137 laudos de mulheres. Resultados: Dos laudos analisados para o seguimento,
22,5% estavam com o seguimento adequado e 77,5% não estavam com seguimento
adequado (conduta inadequada ao diagnóstico e/ou tempo para realização da
conduta não estava adequado), de acordo com os parâmetros estabelecidos na
metodologia (recomendações de seguimento). Considerações
finais: Para tanto, torna-se necessário a ampliação da cobertura
alcançada e a alta cobertura da população alvo, somando-se a isso um programa
de rastreamento organizado e acessível. Construir infraestrutura adequada,
aumentar a rede de profissionais capacitados para atender as demandas desde a
busca ativa das mulheres até a execução dos serviços citopatológicos bem como
do tratamento adequado aos casos diagnosticados.
Palavras-chave: Câncer de Colo Uterino; Controle de
Qualidade; Papiloma Vírus Humano; Rastreamento; Seguimento.
ABSTRACT
Objective: The present study aimed to verify the suitability of
the segment of women with altered reports in the state of Tocantins. Methods:
Cross-sectional, evaluative and documentary study. The present study was
developed in the State of Tocantins, which has the SUS organized by the
principle of regionalization and has 139 municipalities. The regions are: Capim
Dourado, Bico do Papagaio, Amor Perfeito, Bananal Island, Southeast, Cerrado
Tocantins Araguaia, Middle North Araguaia and Cantão. The population adopted
was 29,531 women, estimated from the survey of the number of cytopathological
reports issued during the year 2019. The sample calculation considered the use
of the formula for finite populations, after application of the formula, which
stood at 379 requests and reports of women. Seeking to further expand the
reliability of the data, it was decided to triple the sample size, so the
amount was 1,137 reports from women. Results: Of the reports analyzed for
follow-up, 22.5% had adequate follow-up and 77.5% did not have adequate
follow-up (inadequate conduct for diagnosis and/or time to perform the conduct
was not adequate), according to the parameters established in the methodology
(follow-up recommendations). Final considerations: Therefore, it is necessary
to expand the coverage achieved and the high coverage of the target population,
in addition to an organized and accessible screening program. Build adequate
infrastructure, increase the network of professionals trained to meet the
demands from the active search for women to the execution of cytopathological
services as well as the adequate treatment of diagnosed cases.
Keywords:
Cervical Cancer; Quality Control; Human Papilloma Virus; Tracking; Follow-Up.
RESUMEN
Objetivo: El presente estudio tuvo como objetivo verificar la
idoneidad del segmento de mujeres con informes alterados en el estado de
Tocantins. Métodos: Estudio transversal, evaluativo y documental. El presente
estudio fue desarrollado en el Estado de Tocantins, que posee el SUS organizado
por el principio de regionalización y posee 139 municipios. Las regiones son:
Capim Dourado, Bico do Papagaio, Amor Perfeito, Isla Bananal, Sudeste, Cerrado
Tocantins Araguaia, Medio Norte Araguaia y Cantão. La población adoptada fue de
29.531 mujeres, estimada a partir de la encuesta del número de informes
citopatológicos emitidos durante el año 2019. El cálculo de la muestra
consideró el uso de la fórmula para poblaciones finitas, luego de la aplicación
de la fórmula, que quedó en 379 solicitudes e informes de mujeres. Buscando
ampliar aún más la confiabilidad de los datos, se decidió triplicar el tamaño
de la muestra, por lo que la cantidad fue de 1.137 informes de mujeres.
Resultados: De los informes analizados para el seguimiento, el 22,5% tuvo un
seguimiento adecuado y el 77,5% no tuvo un seguimiento adecuado (conducta
inadecuada para el diagnóstico y/o tiempo para realizar la conducta no fue el
adecuado), según los parámetros establecidos en la metodología (recomendaciones
de seguimiento). Consideraciones finales: Por lo tanto, es necesario ampliar la
cobertura alcanzada y la alta cobertura de la población objetivo, además de un
programa de tamizaje organizado y accesible. Construir infraestructura
adecuada, incrementar la red de profesionales capacitados para atender las
demandas desde la búsqueda activa de mujeres hasta la ejecución de servicios
citopatológicos así como el tratamiento adecuado de los casos diagnosticados.
Palabras clave: Cáncer Cervicouterino; Control de Calidad; Virus del Papiloma
Humano; Seguimiento; Hacer un Seguimiento.
INTRODUÇÃO
O Câncer de Colo Uterino (CCU) é um
importante problema de saúde pública. Segundo a Organização Pan Americana de
Saúde (OPAS), em todo o mundo, o câncer cervical é o quarto câncer mais
frequente em mulheres, com um número estimado de 570.000 novos casos em 2018,
representando 7,5% de todas as mortes por câncer no sexo feminino. Das
estimadas, mais de 311.000 mortes por CCU a cada ano, mais de 85% delas ocorrem
em regiões menos desenvolvidas1.
Quanto à mortalidade, na região Norte
evidenciam as maiores taxas do país, sendo a única com nítida tendência
temporal de crescimento. Em 2017, a taxa padronizada pela população mundial foi
de 12,24 mortes por 100.000 mulheres, representando a primeira causa de
óbito por câncer feminino nesta região2.
O Câncer de Colo Uterino (CCU) decorre da
replicação desordenada do epitélio de revestimento do colo do útero, com
comprometimento de tecido subjacente e podendo invadir órgãos adjacentes ou à
distância. A infecção persistente pelo Papilomavírus humano (HPV) de tipos
oncogênicos é a principal causa desta neoplasia. Esse tipo de câncer inicia-se
a partir de uma lesão precursora, curável na quase totalidade dos casos, visto
que a progressão deste tipo de câncer ocorre de forma lenta e assim passíveis
de serem detectadas3.
A estratégia utilizada nas últimas
décadas, em diversos países, para a detecção precoce deste câncer é o exame
citológico de Papanicolaou, devendo este ser realizado em mulheres na faixa
etária de 25 a 64 anos e que já tiveram atividade sexual. O exame deve ser
feito a cada três anos, após dois exames normais consecutivos, realizados com
um intervalo de um ano e a atenção básica à saúde tem sido a maior porta de
entrada para este serviço4. As etapas do rastreio implicam desde a
identificação e convite às mulheres, garantia dos recursos humanos e materiais,
disponibilização de exames de qualidade, até o seguimento das mulheres
assegurando tratamento e cuidados para aquelas com exames alterados.
O desempenho desses exames depende de
vários fatores que podem estar relacionados com a qualidade do esfregaço, como
também aqueles relacionados com o desempenho do profissional propriamente dito.
O predomínio do trabalho manual é uma característica marcante do exame
citopatológico do colo do útero5. O processo envolvendo a coleta,
fixação e coloração do material até a liberação do resultado pelo laboratório
retrata essa situação. Embora haja no Brasil diretrizes para o rastreamento
para este câncer, não há parâmetros estabelecidos para a programação dos
procedimentos de sua linha de cuidado6.
Diante disso, objetivo do presente estudo
foi verificar a adequabilidade do segmento de mulheres com laudos alterados no
estado do Tocantins.
MÉTODOS
Estudo do tipo transversal, avaliativo e
documental.
O presente estudo foi desenvolvido no
Estado do Tocantins, o qual possui o SUS organizado pelo princípio da
regionalização e possui 139 municípios. Conforme pactuação na CIB de 29 de
agosto de 2012, o Estado do Tocantins é composto por oito Regiões de Saúde,
respeitando os critérios adotados pelo Decreto Federal 7.508/2011 e Resolução
Tripartite 004/20127.
As regiões são: Capim Dourado, Bico do
Papagaio, Amor Perfeito, Ilha do Bananal, Sudeste, Cerrado Tocantins Araguaia,
Médio Norte Araguaia e Cantão.
A população adotada para este estudo foi
de 29.531 mulheres, estimada a partir do levantamento do número de mulheres com
laudos citopatológicos emitidos durante o ano de 20198. O cálculo
amostral considerou a utilização da fórmula para populações finitas proposta
por Viegas9, apresentada a seguir:
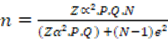
onde:
n= Tamanho (número de elementos) da
amostra;
N= Tamanho (número de elementos) da
população;
P= Prevalência esperada do evento,
percentual com o qual o fenômeno se verifica, onde se adotou 50%, (valor de P=
0,5), por garantir a maior amostra possível;
Q= é o valor complementar de P, ou seja,
50% (valor de Q=0,5) também;
Zα= É o desvio do valor médio que
aceitamos para alcançar o nível de confiança desejado (Nível de confiança 95%,
valor de Zα= 1,96).
e= É a margem de erro máximo que vamos
admitir, 5%, logo valor de e=0,05.
Após aplicação da fórmula, o n ficou em
379 requisições e laudos de mulheres. Buscando ampliar ainda mais a
fidedignidade dos dados, optou-se por triplicar o tamanho amostral, para que a
amostra fosse ainda mais representativa da população, logo o quantitativo ficou
1.137 laudos de mulheres.
Buscou-se ter análise de todas as regiões
de saúde do Tocantins e para tanto, foi realizada a técnica de amostragem
aleatória proporcional estratificada dos laudos citopatológicos para cada
região de Saúde. Essa técnica considera que a população é dividida em
subconjuntos (no presente estudo, as regiões de saúde são os subconjuntos)
homogêneos dos quais os elementos são selecionados aleatoriamente e
proporcional porque considerou proporcionalmente o tamanho do estrato10.
Os levantamentos dos dados deram-se
mediante levantamento documental no banco de dados do SISCAN, de forma
sigilosa, em local fechado e reservado para pesquisa, sob a supervisão,
participação e acompanhamento de uma das pesquisadoras que detém a guarda dos
dados conforme Termo de Fiel Depositário em anexo (TFD).
Além disso, foram capturados os laudos
alterados emitidos via SISCAN, na seção Monitoramento. Fez-se uma análise
referente ao período compreendido entre o primeiro e o segundo laudo (quando
presente) e as condutas utilizadas no seguimento se estavam em conformidade com
as Diretrizes Brasileiras para o Rastreamento do Câncer do Colo do Útero11.
As análises dos dados foram realizadas em
programas estatísticos Software R e SPSS. Inicialmente, os resultados foram
apresentados utilizando-se frequência absoluta e relativa, expressos em
porcentagens, médias, desvio padrão, utilizando estatística descritiva, e
Intervalos de Confiança (IC 95%). Para as variáveis categóricas, utilizou-se o
Teste do Qui- quadrado ou Teste Exato de Fisher para estimar as diferenças
entre os grupos, do laudo com presença de alteração nos laudos (variável
categórica dicotômica SIM/NÃO) e entre as variáveis do laudo alterado com a
adequabilidade do seguimento (variável categórica dicotômica SIM/NÃO).
O projeto de pesquisa foi cadastrado na
Plataforma Brasil, submetido ao Comitê de Ética em Pesquisa (CEP) da UFT e
obteve parecer favorável em 13/07/2020 sob o número do parecer 4.152.647.
Toda a pesquisa foi realizada em conformidade com as diretrizes e normas
regulamentadoras de pesquisas envolvendo seres humanos do Conselho Nacional de
Saúde, segundo resolução 466 de 12.12.201212.
RESULTADOS
Desta forma foram avaliadas 1132 mulheres
cujo perfil demonstrou que a maioria estava dentro da faixa etária preconizada
(25 a 64 anos), a raça predominante foi a não branca, o nível de escolaridade
não foi contemplado, e grande parte residia longe do local de coleta do exame
citopatológico.
Dos 1132 aceitos na análise pré-analítica,
41 (3,6%) foram classificados como amostra insatisfatória. Os motivos foram: 36
(87,9%) artefatos de dessecamento, dois (4,9%) material acelular ou
hipocelular, outros dois (4,9%) por contaminantes externos e um (2,4%) por
presença de sangue em mais de 75% da lâmina. Dessa
forma os laudos válidos para a análise dos fatores associados à presença de
alteração foram 1091.
Dos laudos analisados, 7%
apresentou alguma alteração e todas as regiões tiveram pelo menos um laudo
alterado. A distribuição dos laudos alterados por região territorial do
Tocantins está mostrada no Gráfico 1 e foi 34 (44,6%) na região Capim Dourado,
16 (21,1%) na região Ilha Bananal, 12 (15,8%) na região Médio Norte, 05 (6,6%)
na região do Cantão, 03 (3,9%) na região Amor Perfeito, 03 (3,9%) na região do
Cerrado, 02 (2,6%) na região Bico do Papagaio e 01 (1,3%) na região Sudeste.
Gráfico 1 - Frequência absoluta e
relativa dos laudos que apresentaram alterações. Tocantins, Brasil. 2019.
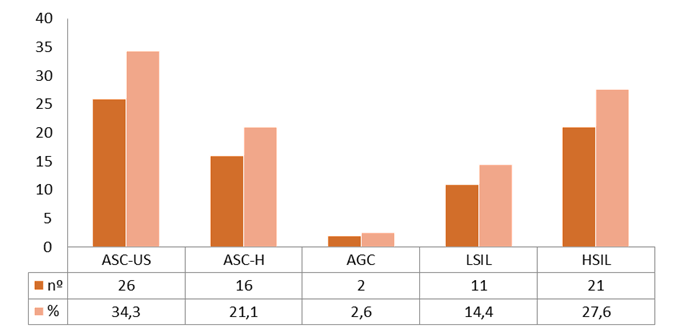
ASC-US: Células Escamosas Atípicas de Significado Indeterminado;
ASC-H: Células Escamosas Atípicas, não se pode excluir HSIL; AGC: Células
Glandulares Atípicas; LSIL: Lesão Intraepitelial Escamosa de Baixo Grau; HSIL:
Lesão Intraepitelial Escamosa de Alto Grau.
Fonte: SISCAN, 2019. Organização: Souza, 2021.
Na presente pesquisa, mais de um epitélio
mostrou associação com o desfecho como apresentado na Tabela 1.
Tabela
1 - Fatores
presentes no laudo citopatológico associados à presença de alteração.
Tocantins, Brasil. 2019.
|
|
Presença de alteração
|
|
|
Sim
n(%)
|
Não
n(%)
|
p-valor
|
RP
|
IC
|
|
Número de epitélios (n=1091)
Um epitélio
Mais de um epitélio
|
10 (1%)
66 (6%)
|
408 (37,4%)
607 (55,6%)
|
0,000*
|
4,4
|
2,25-8,72
|
|
Representatividade da zona
de transformação (n=1091)
Sim
Não
|
66 (6%)
10 (1%)
|
607 (55,6%)
408 (37,4%)
|
0,000*
|
0,2
|
0,11-0,44
|
|
Presença de microbiologia
(n=1091)
Sim
Não
|
73 (6,7%)
03 (0,3%)
|
1012 (92,7%)
03 (0,3%)
|
0,006**
|
0,7
|
0,14-0,36
|
|
Presença de alterações
benignas (n=1091)
Sim
Não
|
73 (6,7%)
03 (0,3%)
|
1012 (92,7%)
03 (0,3%)
|
0,006**
|
0,7
|
0,14-0,36
|
*Teste Qui-quadrado;**
Teste Exato de Fisher
Fonte: SISCAN, 2019. Organização: Souza, 2021.
Dando continuidade à análise dos dados
verificou-se sobre o seguimento das mulheres com laudos alterados. Dos laudos
analisados para o seguimento, 22,5% estavam com o seguimento adequado e 77,5%
não estavam com seguimento adequado (conduta inadequada ao diagnóstico e/ou
tempo para realização da conduta não estava adequado), de acordo com os
parâmetros estabelecidos na metodologia (recomendações de seguimento).
O cruzamento dos laudos alterados com a
adequabilidade do seguimento foi verificado para identificar se algum laudo
específico tinha associação com o seguimento e está apresentada na Tabela 2.
Tabela
2 -
Diagnóstico descrito nos laudos alterados e associação com a adequabilidade do
seguimento. Tocantins, Brasil. 2019.
|
|
Adequabilidade
do seguimento
|
|
|
Sim
n(%)
|
Não
n(%)
|
p-valor**
|
RP
|
IC
|
|
ASC-US
(n=71)
Sim
Não
|
02 (2,8%)
14 (19,7%)
|
23 (32,3%)
32 (45,2%)
|
0,310
|
0,19
|
0,41-0,96
|
|
ASC-H
(n=71)
Sim
Não
|
06 (8,4%)
10 (14,1%)
|
09 (12,8%)
46 (64,7%)
|
0,740
|
3,06
|
0,88-10,5
|
|
AGC (n=71)
Sim
Não
|
00 (00%)
16 (22,5%)
|
02 (2,8%)
53 (74,7%)
|
0,598
|
1,30
|
1,14-1,48
|
|
LSIL (n=71)
Sim
Não
|
00 (00%)
16 (22,5%)
|
10 (14,1%)
45 (63,4%)
|
0,063
|
1,35
|
1,16-1,57
|
|
HSIL (n=71)
Sim
Não
|
08 (11,3%)
08 (11,3%)
|
11 (15,5%)
44 (61,9%)
|
0,022
|
4,0
|
1,22-13,0
|
**Teste Exato de Fisher
ASC-US: Células Escamosas Atípicas de Significado Indeterminado;
ASC-H: Células Escamosas Atípicas, não se pode excluir HSIL; AGC: Células
Glandulares Atípicas; LSIL: Lesão Intraepitelial Escamosa de Baixo Grau; HSIL:
Lesão Intraepitelial Escamosa de Alto Grau.
DISCUSSÃO
Dentre os laudos alterados, cinco
deles não foi possível monitoramento. Isso pode ser explicado pelo fato de a
mulher ser de outro estado brasileiro e ter realizado a coleta no Tocantins, o
que não permite alimentação do sistema, pelo Tocantins. O módulo Seguimento no
SISCAN não concede que o usuário de um estado acesse ou modifique dados de
pacientes de outro estado. Como o Tocantins faz divisa com outros estados (Maranhão e Pará, ao Norte; Goiás, ao Sul;
Maranhão, Piauí e Bahia, ao Leste; Pará e Mato Grosso, a Oeste)
é usual esse tipo de conduta pela população que mora nos limites do estado.
Diferente dos dados apresentados na
presente pesquisa, uma pesquisa do sul do Brasil revelou que em 56,3% da
amostra houve somente a representação do epitélio escamoso, conferindo ausência
da Zona de Transformação (ZT) em mais de metade das amostras. Nas demais, a
representação foi distribuída entre epitélios glandulares e metaplásicos
associados ao epitélio escamoso. Em contrapartida, identificou-se a existência
de associação significativa entre a representação dos epitélios e alterações
anormais. Em 32,7% das amostras com alterações celulares anormais foi
verificada a representação do epitélio escamoso associado ao glandular. Essa
porcentagem foi para 51% quando a presença dos epitélios escamoso, glandular e
metaplásico13. Dessa forma, o estudo em questão corrobora com o
nosso e sugere que amostras com representação do epitélio escamoso associado ao
glandular e/ou metaplásico tem mais chances de detectar lesões precursoras.
De acordo com os fatores presentes no
laudo citopatológico associados à presença de alteração a descrição das
alterações benignas no laudo consiste em: inflamação, metaplasia escamosa
imatura, reparação, atrofia com inflamação, radiação e outros que necessitam
ser especificados no laudo citopatológico. A inflamação sem identificação de
agente é caracterizada por alterações citomorfológicas decorrentes de trauma
físico ou químico, radiação, irritação por DIU ou outras causas não
específicas. Essas alterações celulares associadas à inflamação obedecem aos
critérios a seguir: aumento nuclear de grau variável, os núcleos em geral não
estão sobrepostos, binucleação ou multinucleação, hipocromasia nuclear,
hipercromasia nuclear (porém a cromatina é homogênea), limites citoplasmáticos
bem definidos, o citoplasma pode apresentar vacuolização, policromasia ou halos
perinucleares, os nucléolos únicos ou múltiplos podem estar presentes, as
células aumentadas geralmente formam camadas coesas que se interdigitam em uma
arquitetura clássica de “cardume”14.
A inflamação e a metaplasia escamosa
imatura foram as alterações benignas mais frequentes. A Metaplasia escamosa
imatura mostrou associação estatisticamente significante com alterações
(p=0,000). O processo de metaplasia representa a
substituição de um tipo de epitélio (neste caso endocervical) por outro
(escamoso) como resposta protetora14.
Percebe-se que o fato de a mulher ter
laudo alterado com alterações mais graves, a conduta é adequada. Todavia,
quando as lesões estão em estágios iniciais os profissionais erram nas condutas
o que pode justificar os achados de número de casos elevados, pois a
intervenção precoce adequada não é realizada. Outro fato grave é que as atipias
glandulares, que deveriam ser encaminhadas para colposcopia imediatamente,
foram negligenciadas sem nenhuma conduta adequada.
Reforça-se a preocupação com relação à
cobertura populacional dos exames citopatológicos que é de 1/3 da população
feminina de 25 a 64 anos6 e cujo valor correspondente é de 107.095
mulheres no estado do Tocantins. Em 2019 ficou pactuado (0,56) deste valor que
corresponde à realização de 59.973 exames citopatológicos (SES, 2019).
Entretando o número alcançado de coletas realizadas de PCCU em 2019 ficou em
apenas 29.531
mulheres beneficiadas, muito aquém da meta estabelecida.
CONSIDERAÇÕES
FINAIS
A principal razão para a desigualdade no
CCU quando se compara os países desenvolvidos com os subdesenvolvidos ou em
vias de desenvolvimento é a falta de acesso a exames de qualidade garantidos a
essas mulheres. Para tanto, torna-se necessário a ampliação da cobertura
alcançada e a alta cobertura da população alvo, somando-se a isso um programa
de rastreamento organizado e acessível. Construir infraestrutura adequada,
aumentar a rede de profissionais capacitados para atender as demandas desde a
busca ativa das mulheres até a execução dos serviços citopatológicos bem como
do tratamento adequado aos casos diagnosticados. Entretanto, torna-se
necessária a organização programática e desempenho adequados à realidade da
região norte do Brasil, onde se detectam os maiores índices de CCU.
A implementação do rastreamento universal
do CCU é imprescindível, porém o esforço deve estar associado a um seguimento
adequado. A presente pesquisa detectou que o seguimento no estado do Tocantins
é inadequado. As condutas tardias ou ainda a falta delas corroboram para o
desfecho de altos índices de carcinoma invasivo e de óbitos por CCU na região
norte do país. As recomendações das Diretrizes Brasileiras para o Rastreamento
do CCU não estão sendo seguidas, sendo necessário o treinamento e capacitação
técnica responsável pelo seguimento, desde a alimentação do sistema SISCAN e
convocação das mulheres, ao tratamento adequado.
Nem todo método de rastreamento por si só
alcança grandes êxitos. Como método auxiliar à citologia oncótica, sugere-se a
Inspeção Visual do colo com Ácido Acético (VIA), de baixo custo, muito
utilizado em países com recursos limitados tais como Bangladesh e Índia que
utilizaram esse meio e ampliaram seus programas de rastreamento do CCU
alcançando elevados graus de organização programática e desempenho.
REFERÊNCIAS
1. Organização Pan-Americana da Saúde [Internet]. Available
from: https://www.paho.org/bra/index.php?option=com_content&view=article&id=5634:folha-informativa-hpv-e-cancer-do-colo-do-utero&Itemid=839
2. Santos MO. Estimativa 2018: Incidência de Câncer no
Brasil. Rev Bras Cancerol. 2018 Mar 30;64(1):119–20.
3. Ministério da Saúde (BR). Atenção básica cadernos de
controle dos cânceres do colo do útero e da mama atenção básica cadernos de
controle dos cânceres do colo do útero e da mama [Internet]. 2a ed.
Brasília:
Editora do Ministério da Saúde; 2013. [cited 2022 Jun 27]. Available
from: https://bvsms.saude.gov.br/bvs/publicacoes/controle_canceres_colo_utero_2013.pdf
4. Ministério da Saúde (BR). Protocolos da Atenção Básica: saúde
das mulheres [Internet]. Brasília-DF: Ministério da Saúde; 2016. 2016. [cited
2022 Jun 27]. Available from: https://bvsms.saude.gov.br/bvs/publicacoes/protocolos_atencao_basica_saude_mulheres.pdf
5. Instituto Nacional de Câncer (BR). Manual de Gestão da
Qualidade para Laboratório de Citopatologia [Internet]. Rio de Janeiro: INCA; 2018
[cited 2022 Jun 27]. Available from: https://www.inca.gov.br/publicacoes/manuais/manual-de-gestao-da-qualidade-para-laboratorio-de-citopatologia
6. Instituto Nacional de Câncer (BR). Parâmetros Técnicos para o
Rastreamento do Câncer do Colo do Útero [Internet]. Rio de Janeiro: INCA; 2019.
[cited 2022 Jun 27]. Disponível em: https://www.inca.gov.br/publicacoes/livros/parametros-tecnicos-para-o-rastreamento-do-cancer-do-colo-do-utero
7. Comissão Intergestores Bipartite. Decreto Federal 7.508/2011 e
Resolução Tripartite 004/2012. Secretaria Estadual de Saúde do Tocantins – SES,
2020.
8. Instituto Nacional de Câncer José Alencar Gomes da Silva. Estimativa
2020. Incidência do Câncer no Brasil [Internet]. Rio de Janeiro: INCA; 2019. [cited
2022 Jun 27]. Disponível em: https://www.inca.gov.br/publicacoes/livros/estimativa-2020-incidencia-de-cancer-no-brasil
9. Viegas W. Fundamentos lógicos da Metodologia Científica
[Internet]. 3. Ed. Rev. Brasília: Universidade de Brasília; 2007. [cited 2022
Jun 27]. Available from: https://brapci.inf.br/index.php/res/v/4999
10. Polit DF, Beck CT. Fundamentos de Pesquisa em Enfermagem -
7ed: Avaliação de Evidências para a Prática da Enfermagem [Internet]. Google
Books. Artmed Editora; 2016 [cited 2022 Jun 27]. Available from: https://books.google.com.br/books/about/Fundamentos_de_Pesquisa_em_Enfermagem_7e.html?id=2AKpDAAAQBAJ&redir_esc=y
11. Instituto Nacional de Câncer (BR). Diretrizes brasileiras para
o rastreamento do câncer do colo do útero [Internet]. Rio de Janeiro: INCA;
2018. [cited 2022 Jun 27]. Available from: https://www.inca.gov.br/publicacoes/livros/diretrizes-brasileiras-para-o-rastreamento-do-cancer-do-colo-do-utero
12. Brasil.
Conselho Nacional de Saúde. Resolução n° 466, de 12 de dezembro de 2012. Aprova
normas regulamentadoras de pesquisas envolvendo seres humanos. Brasília: Diário
Oficial da União; 2013. https://bvsms.saude.gov.br/bvs/saudelegis/cns/2013/res0466_12_12_2012.html
13. Ceolin R, Nasi C, Coelho DF, Paz AA, Lacchini AJB. Análise do
rastreamento do câncer do colo do útero de um município do sul do Brasil. Rev
Pesqui (Univ Fed Estado Rio J, Online) [Internet]. 2020 [cited 2022 Jun
27];440–6. Available from: https://pesquisa.bvsalud.org/portal/resource/pt/biblio-1052977
14. Nayar
R. Sistema Bethesda para Relato de Citologia Cervical- Definições, Critérios e
Notas Explicativas. Ritu Nayar; David C. Wilbur. Tradução de Samantha Abreu. 3a
Ed. São Paulo: Livraria Livromed; 2018. 384p.
Todos
os autores contribuíram com a confecção do artigo
Fomento: não há instituição de
fomento
Editor
Científico: Francisco Mayron Morais Soares. Orcid:
https://orcid.org/0000-0001-7316-2519